癌蛋白KRAS的突變發生于約25%的癌癥病例中,且與極差的疾病預后有關,因此,科學家們認為,阻斷KRAS信號是一種潛在的抗癌途徑。然而,先前幾十年的研究證明,該蛋白可能是一種“無成藥性”的靶點,因為,它的表面除了一個GTP結合口袋,其它部分非常光滑,因此,藥物研發人員很難在其表面找到小分子候選藥物的“立足點”(結合口袋)。
知識卡:在細胞內,KRAS與鳥苷二磷酸(GDP)結合時處于失活狀態,與鳥苷三磷酸(GTP)結合時處于激活狀態,而KRAS的異常激活與多種癌癥密切相關。
不過,大約在10年前,研究人員發現,KRAS實際上比想象得更具靶向性,這使得研發靶向KRAS的藥物取得了突破性的進展。如表1所示,至少有5種KRAS調節劑處于臨床開發階段。其中,AMG 510、MRTX849以及JNJ?74699157/ARS-3248這三種候選藥物僅靶向KRAS的G12C突變體(KRAS-G12C),而BI1701963(通過與SOS1結合來抑制KRAS)和mRNA-5671(靶向KRAS蛋白的一種癌癥疫苗)有著不同的作用機制,可能在更廣泛的人群中發揮作用。
知識卡:KRAS的失活與激活受兩類因子的調節:1)鳥嘌呤核苷酸交換因子(GEF,如SOS蛋白),這類蛋白催化KRAS與GTP的結合,從而促進KRAS的激活;2)GTP酶激活蛋白(GTPase-activatingproteins,GAPs),這類蛋白能夠促進與KRAS結合的GTP水解成為GDP,從而抑制KRAS的激活。
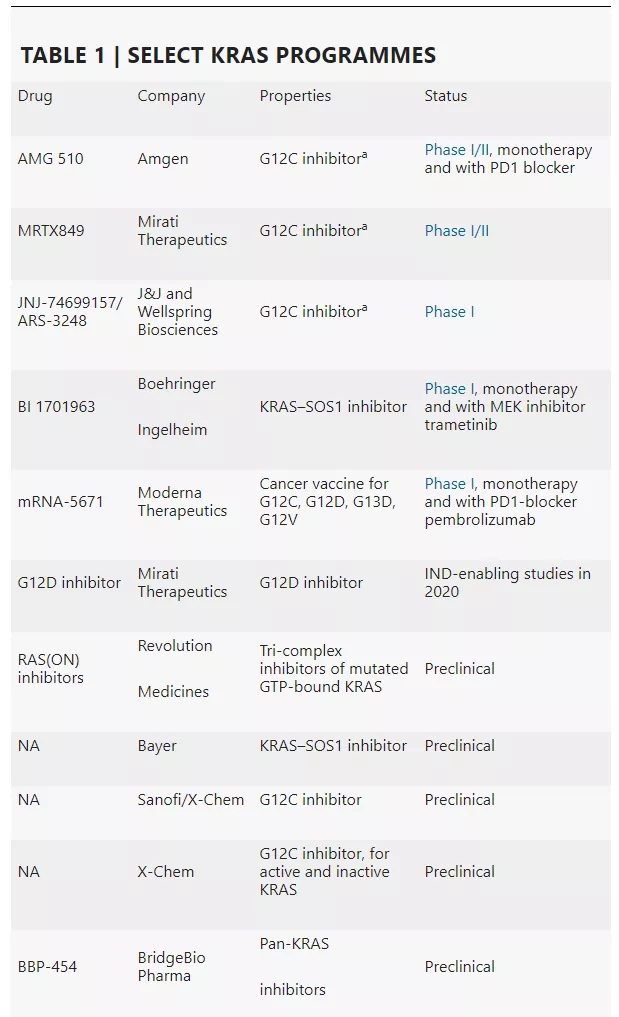
數據來源:Nature Reviews Drug Discovery
一、KRAS-G12C抑制劑
總體來說,KRAS抑制劑的進展與業界對“通過共價相互作用與靶點結合的小分子藥物”的興趣的提升緊密相關。先前很長一段時間,藥物研發人員一直避免使用共價結合劑,因為他們擔心這種混雜且不可逆的結合可能產生脫靶毒性。然而,隨著EGFR抑制劑afatinib、BTK抑制劑ibrutinib等候選藥物證實這種毒性是可控的,許多公司也開始探索這種共價結合劑是否也能適用于其它靶點。
加州大學舊金山分校的化學生物學家Kevan Shoka很早就發現了開發KRAS共價結合劑的可能性。因為,他們發現,KRAS-G12C突變體的特征是新引入一個半胱氨酸,而這種親核氨基酸很容易形成共價鍵,如果一類小分子可共價結合KRAS-G12C突變體中的半胱氨酸,那么,它們就有望用于治療攜帶這類KRAS突變的患者。
知識卡:G12C突變是最常見的KRAS突變之一,具體指KRAS 12位的甘氨酸(glycine)突變為半胱氨酸(cysteine)。該突變存在于約13%的肺腺癌中,3%的結直腸癌中以及2%的其它實體瘤中。其它常見的KRAS突變包括G12D、G12V,它們在結直腸癌和胰腺癌中表達水平很高。
2013年,在一篇Nature論文中[1],Shokat首次報道了利用小分子共價結合KRAS-G12C突變體的可行性(為了獲得這類分子,其團隊堅持了6年的篩選)。通過晶體學分析,Shokat等發現,共價化合物可與KRAS上先前未被發現的“開關-II口袋”(switch-II pocket)結合。
三大候選藥物
這一發現立即引起了轟動。之后,Shokat與人聯合創辦的Araxes Pharma的子公司Wellspring Biosciences證實,Shokat所鑒定的這一化合物的改良版本可縮小被移植了攜帶KRAS-G12C突變的人類腫瘤的小鼠的腫瘤。不久后,Araxes與強生旗下的Janssen達成合作,致力于將這一候選藥物(前文提到的JNJ?74699157/ARS-3248)推進臨床試驗。
在Araxes取得進展的同時,制藥巨頭Amgen也有了重要收獲。通過與Carmot Therapeutics合作,他們很早就發現,一些共價結合化合物甚至可以打開“開關-II口袋”的“蓋子”(lid)上的一個“神秘口袋”。
“這是我們的一個關鍵發現。打開這一神秘口袋可能為候選分子帶來更多潛在的結合位點。”Amgen研究副總裁Margaret Chu-Moyer說。(2017年,Shokat及其同事在Cell Chemical Biology雜志上報道了他們發現的同一個“神秘口袋”[2])
2018年8月,Amgen首個KRAS-G12C抑制劑(AMG510)進入臨床研究,幾個月后(2019年1月),競爭對手MiratiTherapeutics的KRAS-G12C抑制劑MRTX849也開始人體試驗,Araxes和Janssen的JNJ-74699157在今年7月緊隨其后。
Amgen公司不久前(9月)在ESMO上公布了AMG 510 I/II試驗的初步數據。13例接受AMG 510治療的NSCLC患者中,有7例(54%)患者獲得了部分緩解,腫瘤體積變小;其他6例患者接受治療后病情穩定。此外,患者似乎對AMG 510耐受良好,迄今為止未顯示劑量限制毒性。目前,多例患者已經接受AMG 510治療超過6個月。
Amgen腫瘤開發負責人GregFriberg認為,由于參與該試驗的NSCLC患者病情都已惡化,且AMG 510平均是他們的四線治療,因此,這些初步數據提示,這一KRAS-G12C抑制劑響應持久性良好。
不過,Amgen針對結直腸癌患者的試驗的早期結果不算“亮眼”。12例接受治療的患者僅1例(8%)部分緩解,剩余10例患者病情穩定。Friberg表示,不同癌種中AMG 510療效的差異可能反應了在不同疾病中,KRAS-G12C通路起著略微不同的作用。
Mirati公司在10月于AACR-NCI-EORTC會議以及Cancer Discovery雜志上[3]公布了MRTX849相關的數據。6例可評估的NSCLC患者中,3例(50%)達部分緩解;4例結直腸癌患者中,1例(25%)達部分緩解。
聯合治療
除了單藥治療,開發者們也已在研究基于KRAS-G12C抑制劑的聯合治療。比如,安進正在研究AMG 510與PD-1抗體pembrolizumab的聯合。在10月30日發表于Nature上的一篇論文中[4],相關研究者證實,10只接受這種聯合策略治療的小鼠中有9只腫瘤永久消失了。此外,被“AMG 510+pembrolizumab”治愈的小鼠之后還擁有了排斥KRAS-G12D腫瘤的能力,表明這種聯合治療可能會驅動一種獲得性免疫反應。
目前,Amgen已經在NSCLC患者中測試這一聯合治療策略,且計劃在今年年底在結直腸癌患者中進行測試。Mirati也計劃將MRTX849與pembrolizumab聯用。
除PD-1抗體,SHP2抑制劑是KRAS-G12C抑制劑開發商為它們尋找的另一“聯合伙伴”。SHP2是一種磷酸酶,與KRAS的激活-失活機制有關。本月初,安進剛剛與一家名為Revolution Medicines的公司達成合作,獲得其實驗性SHP2抑制劑RMC-4630,不過,調查“AMG 510+ RMC-4630”的試驗何時開始尚未披露。Mirati此前已與諾華達成合作,開發“SHP2抑制劑TNO155+ MRTX849”組合療法,相關I/II期試驗計劃在2020年進行。
其它在研的組合策略包括“KRAS-G12C抑制劑+CDK4抑制劑”。利用全基因組CRISPR干擾篩選,Shokat團隊最近發現,當KRAS被抑制時,CDK4是那些對細胞生存至關重要的基因之一。他希望,調查這一組合策略的試驗盡快開始。
二、靶向其它KRAS突變體
除了KRAS-G12C抑制劑,業界在開發針對其它KRAS突變的藥物方面也取得了重要進展。其中,名為ModernaTherapeutics的公司正在與默沙東合作,開發一種mRNA癌癥疫苗(表1及前文提到的mRNA-5671),使其能夠在體內制造抗原,以啟動T細胞尋找和破壞表達四種關鍵KRAS突變體(G12C、G12D、G12V和G13C)的細胞。
在一項I期試驗中,Moderna和默沙東正在攜帶KRAS突變或轉移性的NSCLC、結直腸癌或胰腺癌患者中測試mRNA-5671單藥治療和“mRNA-5671+ pembrolizumab聯合治療”的潛力。
此外,如表1所示,Mirati 計劃于2020年開展向FDA遞交G12D抑制劑 IND申請所需的研究。
三、間接抑制KRAS
針對泛KRAS(pan-KRAS)的藥物在近期也取得了令人興奮的進展。10月末,勃林格殷格翰(BI)宣布,其首個泛KRAS抑制劑BI1701963進入臨床開發階段。BI1701963靶向的是SOS1蛋白,該蛋白可促進KRAS的激活。臨床前研究表明,這種高度特異性的SOS1抑制劑可降低細胞和動物模型中KRAS-GTP水平和MAPK信號。所有的早期跡象均表明,BI1701963對KRAS激活突變有廣泛的抑制作用。
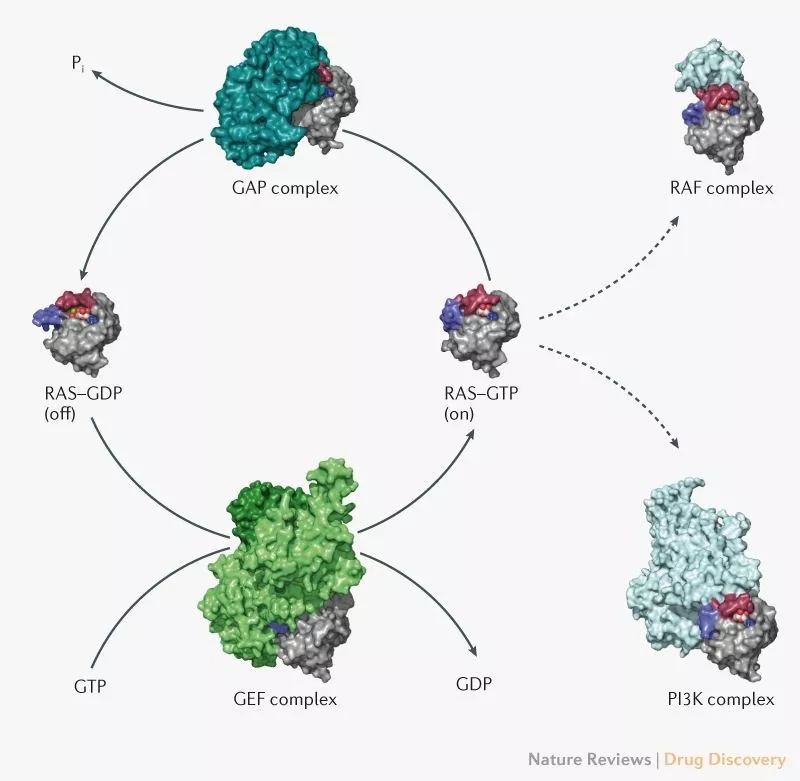
KRAS與GTP結合時處于“開啟”狀態,與GDP結合時處于“關閉”狀態,其構象在不同狀態時有所不同,這種不同調節了其結合“伙伴”的能力,如SOS1、PI3K、RAF以及GAPs.(圖片來源:Nature Reviews Drug Discovery)
“與KRAS-G12C抑制劑不同,SOS1抑制劑類化合物阻斷的是SOS1-KRAS的相互作用,因而與KRAS是何種突變無關。”BI癌癥研究負責人Norbert Kraut解釋道。
不過,BI已發現,SOS1抑制劑單藥治療效果并不突出,只能讓腫瘤“停滯”,而不能殺傷腫瘤。為了獲得腫瘤細胞殺死活性,他們必須將BI1701963與MEK抑制劑(trametinib)聯合使用。公司期望,這種聯合策略可提高療效,并潛在的延緩適應性耐藥的出現。
除BI外,今年2月,在一篇PNAS論文中[5], 拜耳也宣布,其發現了一款選擇性抑制KRAS-SOS1相互作用的SOS1結合物。據稱,公司正在研發SOS1抑制劑,但尚未公布任何研發時間表。
四、未來其它可能性
最后,值得一提的是,除間接抑制KRAS的SOS1抑制劑BI1701963外,BI手中還有另一款與KRAS上被新鑒定出的口袋——開關I/II口袋(switch I/II pocket)[6]結合的小分子BI-2852。研究表明,這一新發現的口袋有望為阻斷KRAS與其所有“激活伙伴”(activatingpartners)、效應蛋白和失活蛋白的相互作用帶來可能。BI正在積極推進結合這一口袋的化合物的研發。
鑒于過去幾十年制藥界對靶向KRAS的強烈渴望,相信這些新口袋的發現將進一步助長KRAS藥物的研發熱潮。
小結
領域:KRAS
雜志:Nature Reviews Drug Discovery
亮點:最近兩年,直接或間接靶向KRAS的藥物的研發取得了突破進展。目前,至少有5種KRAS調節劑處于臨床開發階段,包括三種KRAS-G12C突變體抑制劑,一種mRNA癌種疫苗以及一種SOS1抑制劑。最新發表在Nature Reviews Drug Discovery上的一篇文章詳細總結了KRAS領域的近期進展,并分析了目前的競爭格局。Amgen、Mirati、Araxes/Janssen、Moderna 以及BI等公司處于領先地位。
相關論文:
[1] Jonathan M. Ostrem et al. K-Ras(G12C)inhibitorsallosterically control GTP affinity and effector interactions. Nature(2013).
[2] Daniel R. Gentile et al. Ras BinderInduces a Modified Switch-II Pocket in GTP and GDP States. Cell ChemicalBiology(2017).
[3] James G. Christensen et al. The KRASG12CInhibitor, MRTX849, Provides Insight Toward Therapeutic Susceptibility of KRASMutant Cancers in Mouse Models and Patients. Cancer Discovery(2019).
[4] Jude Canon et al. The clinicalKRAS(G12C) inhibitor AMG 510 drives anti-tumour immunity. Nature(2019).
[5] Roman C. Hillig et al. Discovery ofpotent SOS1 inhibitors that block RAS activation via disruption of theRAS–SOS1interaction. PNAS(2019).
[6] Dirk Kessler et al. Drugginganundruggable pocket on KRAS. PNAS(2019).
參考資料:
1# Cracking KRAS(來源:Nature Reviews Drug Discovery)
2# KRAS抑制劑頻獲突破,“不可成藥”靶點將成為歷史?(來源:藥明康德)
3# 勃林格殷格翰將首個泛KRAS抑制劑BI1701963推進至臨床試驗階段,中國將參與全球早期同步開發(來源:醫藥魔方)
4# Nature里程碑:KRAS抑制劑+PD-1,治愈腫瘤有希望(來源:醫藥魔方Pro)
(來源于:醫藥魔方Pro,作者曼話)


